背景/引言:
肝癌是全球公认的重大健康问题, WHO最新全球癌症数据显示:中国肝癌新发病例数37万例,高居中国癌症发病率第4位;死亡病例数32万例,死亡率高居第2位,统计数据显示,肝癌在中国的发病率和死亡率均高于全球平均水平。
近年来,因冷冻消融具有可视、无痛、安全、免疫增强等优点,在肝癌的临床应用中逐渐得到重视和应用。现通过专家共识和相关文献简述冷冻消融技术在肝癌治疗中的进展和疗效。
研究一
冷冻消融治疗的路径有经皮、腹腔镜及开腹3 种方式,临床常用影像引导经皮入路。本共识规范了影像引导下肝癌冷冻消融治疗的患者选择和技术操作流程,提高治疗效果、减少手术风险性,为临床实践和规范肝癌的冷冻消融治疗提供参考。本文将对该专家共识的关键内容进行简述。(1)肝癌直径≤ 5cm,或3 ~ 5 个肿瘤、最大直径≤ 3cm;
(2)原发性小肝癌拒绝外科手术者,或单发肿瘤外科手术后发现切缘有残余或复发者;
(3)转移性肝癌病灶超过3 个无法外科切除,且原发部位肿瘤能够得到有效治疗者;
(4)无血管、胆管和邻近器官侵犯;
(5)肝功能分级Child-Pugh A/B 级,或经保肝治疗达到该标准;
(6)不能手术切除的直径> 5cm的单发肿瘤或直径> 3cm 的多发肿瘤,可行姑息性消融或与经导管动脉栓塞化疗等其他治疗方法联合治疗。术前应详细询问病史并对患者进行全面检查,以评估患者全身情况及对手术的耐受性,确定治疗方案、引导方式、患者及家属的理解和同意。值得注意的是,患者需具备两周内的肝脏超声造影、强化CT 或MRI 检查,必要时行PET-CT检查,用以明确病灶与血管、胆管及周围重要组织器官的关系,并预先设计进针路线、消融范围及冷冻探针组合模型。(1)设计进针路径时,应注意避开肋骨、胃、肠及胆囊等结构,避免术中冷冻能量沿探针传递损伤空腔脏器,导致胆瘘及肠瘘;
(2)如果冷冻治疗应用CT 或MRI 进行术中引导及监控,则术前应锻炼患者呼吸配合,每次扫描时屏气幅度一致,平静呼气末屏气最常应用;
(3)包膜下肝癌,穿刺路径设计应经过部分正常的肝组织,减少肿瘤破裂出血及腹腔内播散的机会;
(4)治疗近膈顶的肝癌,尽可能经肋膈角下方进针,避免探针经过肋膈角、膈肌,损伤肺组织,且冷冻过程中注意控制消融范围,必要时采取水隔离技术,勿伤及膈肌;
(5)靠近腹壁的病灶进行冷冻治疗,应在体表穿刺点敷温水囊,避免冻伤腹壁和皮肤;
(6)靠近胆囊及胃肠道的病变冷冻治疗时,术中监控病变,使冷冻冰球外缘勿达到胆囊和胃肠,防止冻伤后穿孔;
(7)靠近大血管的病变进行手术时,需应用较多数目的冷冻探针,因大血管能够迅速带走冷冻能量,使形成的冷冻冰球较小,影响治疗效果;
(8)直径3 ~ 5cm 但影像学检查显示边界不清呈浸润性生长的病灶,冷冻消融范围应相应扩大,超过病变显示范围1.5cm 以上;
(9)直径> 5cm 的病灶,可通过多针穿刺和多点布针的方法尽可能适形、全面地消融病灶,也可根据情况行姑息性治疗,部分灭活肿瘤、减轻肿瘤负荷或延缓病情进展,以延长患者生存时间和提高生存质量。推荐方案是在消融后1 个月左右,复查动态增强CT 或MRI,或超声造影以评价消融效果,通过观察有无肿瘤残留,可分为完全消融及不完全消融。在肿瘤标志物检查中,原发性肝癌以血清甲胎蛋白水平作为评价指标,转移性肝癌多以癌胚抗原作为评价指标。治疗的不良反应主要有术后寒战发热、肝区疼痛、血清酶升高和血小板减少等,并发症包括感染、出血、胸腔积液、皮肤冻伤、肋间神经损伤、冷休克、胆瘘和肠瘘、肝功能衰竭等。充分术前准备、严格操作规范、准确定位与穿刺及术中动态监控是减少并发症发生率的重要方法。近年来,局部消融治疗得到广泛应用,其具有对肝功能影响少、创伤小、疗效确切、重复性好等特点。研究显示对于直径≤ 3cm 的肝细胞癌,局部消融与外科手术疗效无明显差异,冷冻消融使不适合手术切除的肝癌患者获得根治机会,现已是肝癌局部消融的常用方法。临床常见的原发性肝脏肿瘤是肝细胞癌,局部消融治疗现已是极早期和早期肝细胞癌患者治疗的一个组成部分。局部消融包括射频消融、微波消融和冷冻消融等。与其他方式相比,冷冻消融具有明显优点,包括影像监测冰球的边界、可激活有效的免疫效应、降低血管和其他关键结构损伤的发生率以及避免剧烈疼痛。本文探究了冷冻消融肝癌的临床有效性和安全性。回顾性纳入2018年10月至2019年8月期间接受冷冻消融手术的肝脏肿瘤患者9例, 5 名男性和 4 名女性。中位年龄为66 岁(范围:45-76 岁;平均年龄:62.4 岁)。其中7 例患者患有肝细胞癌,2 例患者患有肝转移癌。1例肝细胞癌患者有2个病灶,其余患者只有1个病灶。根据肿瘤位置,5个肿瘤位于胆囊附近,2个肿瘤位于右门静脉附近,2个肿瘤位于肝包膜附近,1个肿瘤位于胃附近。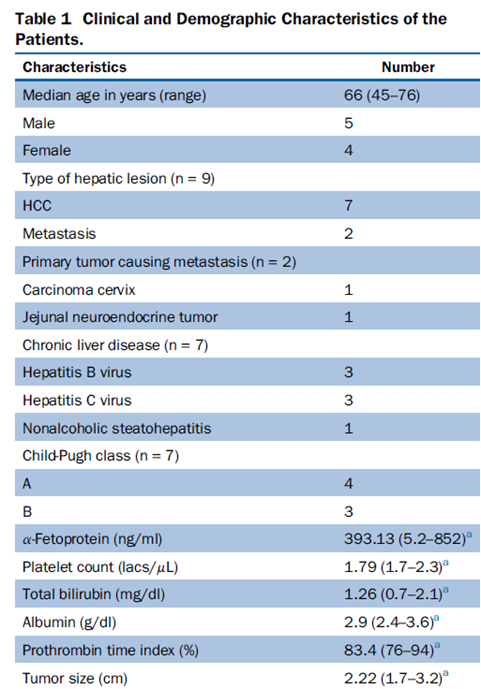
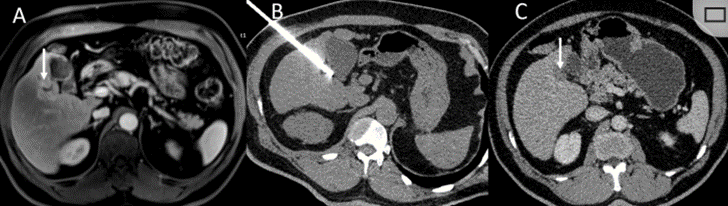
冷冻消融胆囊附近肿瘤病灶
(A)动脉期 MRI 显示胆囊附近有外周增强病变(箭头)。
(B)手术过程中 CT 显示冷冻探针位于病灶内。
(C)消融后,术后 1 个月CT 显示完全消融(箭头)。
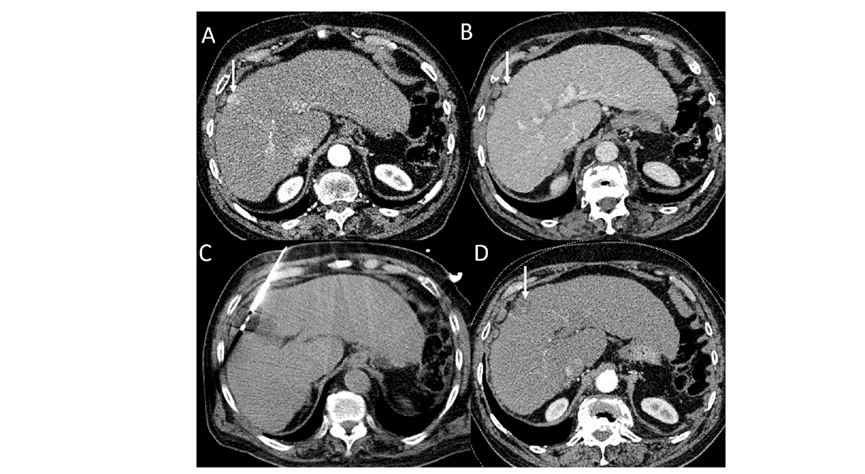
(A)动脉期CT图像显示有一个包膜下结节(箭头)。(C) 在手术过程中的CT显示一个冷冻探针位于病灶内。随访时间中位数为7个月(范围:3-12个月),随访期间患者无局部肿瘤进展或死亡。
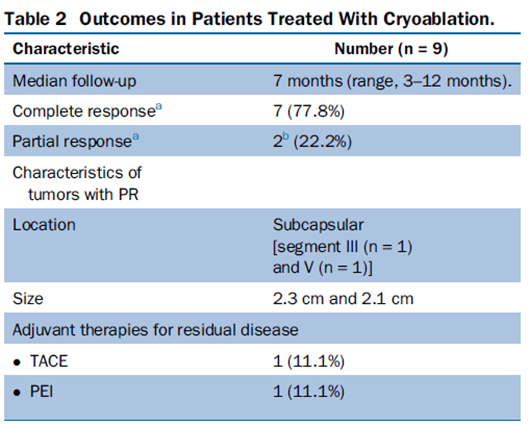
技术成功率为100%,本研究中77.8%(7/9)的患者达到了完全消融,辅助局部治疗后,所有患者均完全消融。
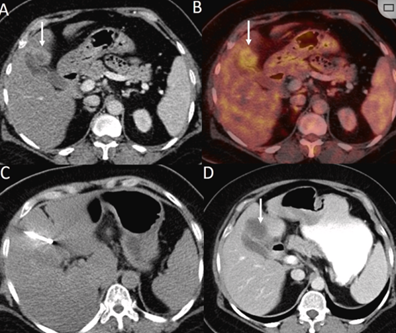
(A)门静脉期 CT 图像显示胆囊附近有病变(箭头)。(D)消融手术后 1 个月CT 显示完全消融。
本研究中患者随访期间无局部肿瘤进展,无死亡病例,没有发现与手术相关的并发症。证实冷冻消融是一种有效的治疗方式,在技术上是可行和安全的。由于肝包膜下病变位置特殊,射频消融有出血及肿瘤种植的风险,可能会对邻近器官造成损伤,并且增加局部肿瘤进展的风险。近年来,冷冻消融术的应用逐渐广泛,有研究显示冷冻消融治疗具有明显优势,可治疗特殊部位的肝肿瘤。本研究的目的是评价冷冻消融治疗肝包膜下肿瘤的安全性和有效性。回顾性纳入2016年7月1日至2018年9月1日期间冷冻消融的57例患者。包括42例男性和15例女性,平均年龄为62.4岁(范围:48-82岁)。每个患者有1个或2个平均肿瘤尺寸为2.4cm的病变(范围:0.6-4.0cm)。所有患者均患有慢性肝病或肝硬化,并伴有乙型肝炎(n=52)、丙型肝炎(n=3)和其他肝炎(n=2)。根据肿瘤位置,在膈肌或肝脏下附近有18个病变(26.5%),胃或肠附近有9个病变(13.2%),腹壁附近有33个病变(48.5%),肾脏附近有8个病变(11.8%)。
入选标准:
(1) 最多3个直径5 cm的肿瘤病变;
(2) 肝功能分级Child-Pugh A/B级患者,无证据表明脏器粘连,无大血管浸润和肝外转移;
(3) 凝血功能:正常凝血酶原时间和血小板计数≥50000 cells/mL;
(4) 年龄<85岁;
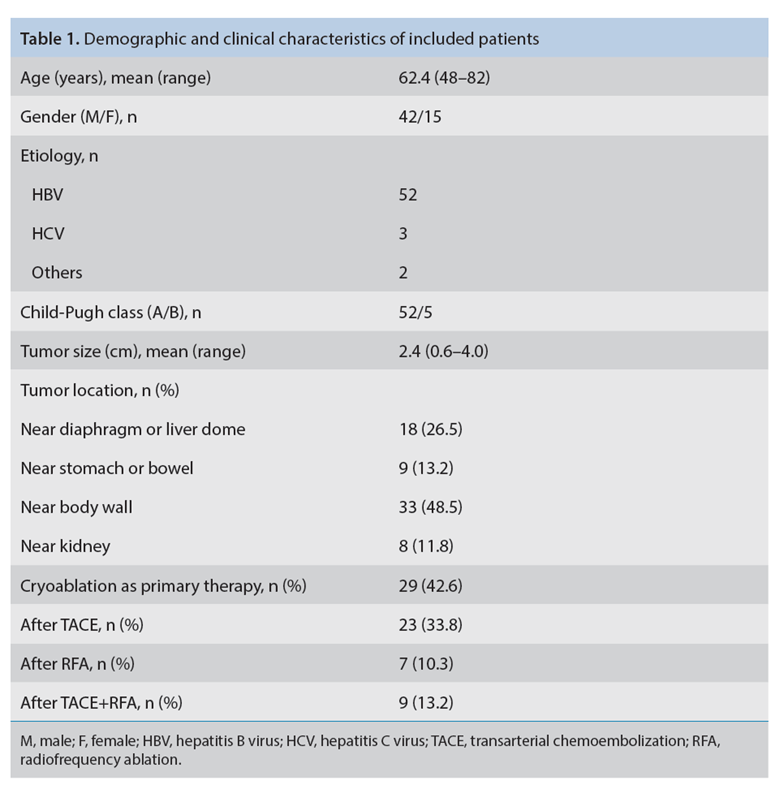
CT引导的冷冻消融
完全消融率为97%(66/68);2名患者均接受了额外的冷冻消融,随后实现完全消融。平均随访期为 12.8 个月(范围:3-27 个月)。所有患者均接受影像复查(CT 或 MRI)。11个病灶(16.2%)检测到局部肿瘤进展,6、12和18个月时的累积局部肿瘤进展率分别为4%、8.2%和20.5%。8例出现远处肝内或肝外病变的患者接受经动脉化疗栓塞、经动脉化疗栓塞加射频消融治疗或全身化疗。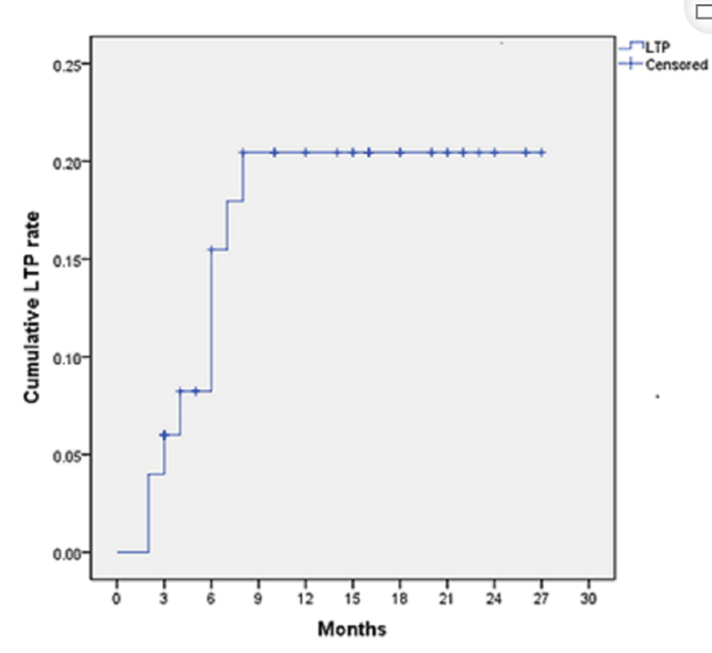
主要和次要并发症发生率分别为3.5%(2/57)和22.8%(13/57)。并发症主要表现为局部皮肤冻伤、中度气胸、发热,仅有少数患者接受治疗,多数患者自行恢复。所有患者能耐受围手术期疼痛,VAS 评分范围在 1-3 分之间(平均 1.65分)。3例患者术后疼痛加重,VAS评分达到4~5分,患者口服止痛药后逐渐缓解。所有患者术后1天血常规、白细胞计数均升高,血小板均有不同程度下降,但变化值均在正常范围内。肝功能1个月后逐渐恢复到正常水平。
手术前后实验室检查结果的变化
(1)经皮冷冻消融治疗包膜下肝细胞癌(HCC)安全有效。(2)经皮冷冻消融治疗包膜下 HCC 的手术过程简单。(3)包膜下 HCC 患者通过冷冻消融治疗可减轻疼痛,并且仅需局部麻醉。冷冻消融是一种微创治疗方法,可用于治疗原发性和转移性肝癌,对于不适合肝切除或肝移植的患者,冷冻消融在临床上得到广泛的应用。本研究的目的是评估冷冻消融对肝细胞癌和肝转移癌患者的有效性。
回顾性纳入2015 年至 2020 年期间49 名患者,23 名男性和 26 名女性。平均年龄为 67.5 岁(范围 44-85 岁)。平均随访时间为 19.8 个月(范围 1-60 个月)。对 54 个肿瘤病灶进行了 64 次 冷冻消融 手术(50 个转移癌和 14 个 HCC)。平均肿瘤直径为 2.15 cm(范围 0.5-5 cm)。肝脏转移灶来自结直肠 (n = 23)、乳腺 (n = 12)、胰腺 (n = 7)、肺 (n = 3)、甲状腺 (n = 2)、胃 (n = 1)、卵巢 (n = 1) 和宫颈癌 (n = 2)。
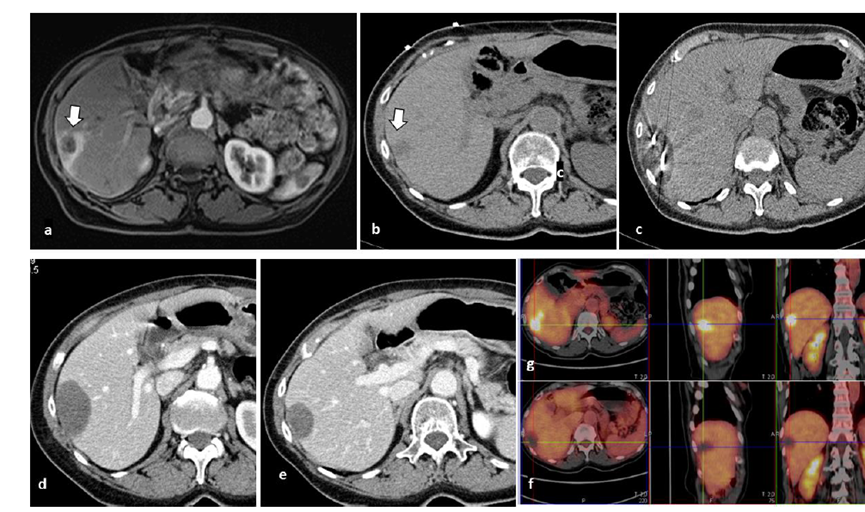
79 岁男性,肝转移(结直肠癌)肿瘤的完全消融病例
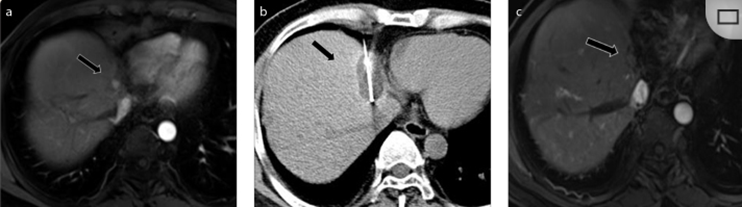
( a ) 轴向 MRI 和 ( b ) 轴向 CT 显示肝S8段有一个16mm的病灶,邻近肝缘。( c )冷冻消融期间CT显示放置了2个冷冻探针,低密度冰球包围病灶。(d)术后1个月随访 CT显示冰球对应的坏死区域,未见复发。(f)与基线影像(g)相比,12个月后的FDG-PET/CT显示未见FDG摄取。
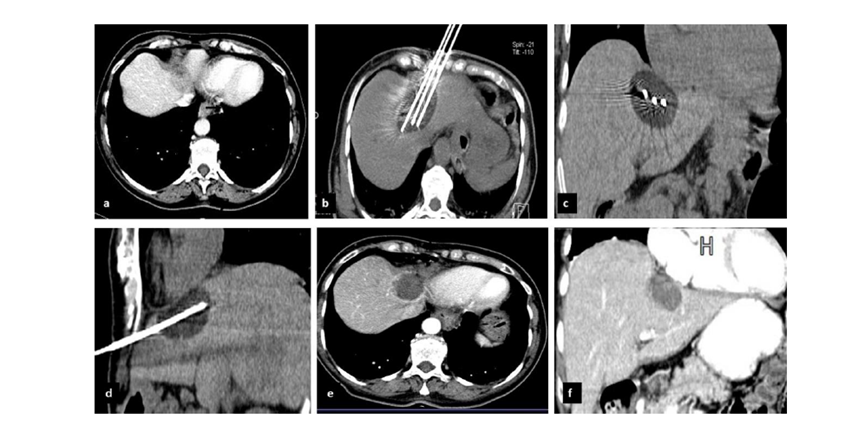
(a)轴向CT显示病变位置毗邻心脏和上腔静脉(黑色箭头)。1个月后的轴向(e)和冠状位(f)增强CT扫描显示低密度区域,由于肉芽组织反应引起的边缘增强。
技术成功100%,92% 的病灶中观察到肿瘤完全消融。16 名患者 (33%) 出现局部复发。10 名患者 (20%) 因局部复发或肿瘤消融不完全而接受二次冷冻消融术。

7名患者出现轻微并发症,未发现脓肿形成、胆漏、胆汁瘤或血液学变化。冷冻消融可安全、有效治疗毗邻重要脏器的原发性肝脏肿瘤和肝转移瘤患者,有效控制肿瘤局部进展,使患者生存获益。我国作为肝癌大国,对于肝癌的治疗一直给予高度重视。基于专家共识和相关文献研究结果显示,冷冻消融技术具有高效、低成本、创伤小、适应证广、并发症相对较少等优点,可有效延长患者生存期、提高生活质量、降低患者经济负担。因此,冷冻消融技术在肝癌的应用中有着极高的潜力和广泛的发展空间。